Vurdering af holdbarhed ud fra de kliniske krav til analysens nøjagtighed
(Af Lektor, Ph.d. Troels Wind)
Kilder
De følgende forslag til vurdering af prøvematerialers holdbarhed stammer primært fra artiklen ”Prøvematerialets holdbarhet – kriterier og vurderinger” af Arne Åsberg m.fl., Klinisk Biokemi i Norden 2011:4:34-38, og til dels fra instruksen ”71.1.1 Analysevalideringer”, versionsnr. 6, af Søren Ladefoged og Niels Tørring (2012), Klinisk Biokemisk Afdeling, Aarhus Universitetshospital.
Det skal understreges, at der er alternative fremgangsmåder til vurdering af holdbarhed, der kan være (mindst) lige så velegnede.
Vurdering af holdbarhed ved hjælp af et gennemsnit af analysesvar og kravet til korrekthed
Kvalitetskravet til en analyses korrekthed defineres oftest som den maksimale bias (\(bias_{max}\)), der ikke har klinisk betydning. Det er derfor nærliggende, at bruge \(bias_{max}\) som grænse for, hvor meget et analyseresultat må ændre sig som følge af opbevaring af prøvematerialet. Med andre ord: Så længe ændringen af analyseresultatet på grund af opbevaring er signifikant mindre end den maksimale tilladte bias, har det næppe klinisk betydning, og prøvematerialet vurderes at være holdbart.
Fremgangsmåden er typisk, at et antal patientprøver analyseres hurtigst muligt for at fastlægge en udgangsværdi, og derefter genanalyseres på relevante tidspunkter. Da den maksimale acceptable bias oftest anføres i procent (\(bias\%_{max}\)), er det fordelagtigt at omregne alle analysesvar til procent af udgangsværdien, således at en eventuel ændring kan sammenlignes direkte med \(bias\%_{max}\). Disse analysesvar i procent kaldes relative analysesvar i det følgende. For hvert tidspunkt beregnes gennemsnittet af de relative analysesvar for patientprøverne, og det vurderes, om ændringen i forhold til udgangsværdien (100%) er større end \(bias\%_{max}\). Vurdering bør ske ud fra et plot, der viser gennemsnittet af de relative analysesvar ved hvert tidspunkt, samt grænserne, der afspejler \(bias\%_{max}\). Fremgangsmåden illustreres med følgende eksempel.
Eksempel
Man har målt P-ALAT på syv plasmaprøver umiddelbart efter centrifugering og afpipettering (udgangsværdien), og igen efter 1, 2, 3 og 4 døgns opbevaring ved 21°C. Rådata (fiktive) kan hentes her. For hver prøve omregnes alle analysesvar til procent af udgangsværdien ved hjælp af følgende ligning:
$$\textit{relativt analysesvar(%)} = \frac{\textit{Analysesvar}}{\textit{Udgangsværdi}}\cdot 100\%$$
Gennemsnittet af de relative analysesvar de enkelte dage er opsummeret i Tabel 1.
Kvalitetskravet til korrektheden for P-ALAT, som definerer grænserne for den tilladelige relative ændring, vælges til \(bias\%_{max} = \pm 11,4\%\) (www.westgard.com/biodatabase1.htm).
Tabel 1. Gennemsnittet (n=7) af de relative analysesvar efter opbevaring af patientprøver ved 21°C det anførte antal døgn.
Gennemsnittet af de relative analysesvar som funktion af tidspunktet, samt grænserne dikteret af kvalitetskravet til korrektheden (\(Udgangsværdi\pm bias\%_{max}\)), er præsenteret i Figur 1.

Figur 1. Gennemsnittet (n=7) af de relative analysesvar for P-ALAT efter opbevaring af patientprøver ved 21°C er indtegnet med grønne krydser. For hvert gennemsnit er indtegnet et 90%-konfidensinterval, baseret på analyseusikkerheden. Grænserne defineret af den maksimale acceptable bias% for analysen er indtegnet som grønne stiplede linier.
Den simplest mulige fortolkning af Figur 1 er, at hvis det gennemsnitlige relative analysesvar ligger uden for \(bias\%_{max}\) grænsen, så er prøvematerialet ikke holdbart i det pågældende tidsrum. Ud fra den vurdering, er plasmaprøver holdbare i 3 døgn ved 21°C for P-ALAT.
Inddragelse af analyseusikkerheden
Men bør dog inddrage analyseusikkerheden i denne fortolkning; det kan jo være en tilfældighed, altså skyldes analyseusikkerheden, at de gennemsnitlige relative analysesvar ligger lige indenfor \(bias\%_{max}\) grænsen efter tre døgn (se Figur 1). Dette kan vurderes ved at beregne et 90%-konfidensinterval for hvert gennemsnit, og vurdere dette intervals beliggenhed i forhold til grænserne.
Beregningen foretages med følgende formel:
$$90\%-\textit{Konfidensinterval}=\textit{gennemsnit af relative analysesvar} \pm 1{,}65\cdot \sqrt{2}\cdot\frac{CV\%_{ana}}{\sqrt{n}}$$
hvor \(CV\%_{ana}\) er analyseusikkerheden og \(n\) er det antal prøver, man har med i sit forsøg.
Der gælder nu, at
- Hvis hele konfidensintervallet ligger inden for grænserne, er prøvematerialet holdbart i det pågældende tidsrum (signifikansniveau 5%)
- Hvis hele konfidensintervallet ligger uden for grænserne, er prøvematerialet ikke holdbart i det pågældende tidsrum (signifikansniveau 5%)
- Hvis en af grænserne er indeholdt i konfidensintervallet, er prøvematerialet hverken signifikant holdbart eller signifikant uholdbart; det er et tvivlstilfælde.
Denne fremgangsmåde svarer til, at man for hvert tidspunkt udfører en t-test for at undersøge, om den gennemsnitlige relative ændring er signifikant mindre end \(bias\%_{max}\). Hvis dette ikke er tilfældet, vurderes det, at prøvematerialet ikke er holdbart. Testen er enkeltsidet, derfor benyttes et 90% konfidensinterval, således at signifikansniveauet for den enkelte test er de sædvanlig 5%.
Det skal understreges, at denne fremgangsmåde kan kritiseres, da den består af et større antal test, én for hvert tidsrum, hvorved det samlede signifikansniveau principielt bliver markant højere end 5%. Dette kan til dels negligeres, såfremt man er omhyggelig i tolkningen af den grafiske præsentation: Kun hvis der er en tilpas overbevisende ændring af analysesvarene i samme retning i løbet undersøgelsen, er det forsvarligt at definere holdbarheden som beskrevet ovenfor.
Eksempel - fortsat
Lad os vende tilbage til eksemplet med P-ALAT og inddrage analyseusikkerheden \(CV\%_{ana} = 2\%\) i fortolkningen. Konfidensintervallerne kan beregnes med følgende resultat (husk, at n = 7):
$$\textit{90%-Konfidensinterval}=\textit{gennemsnit af relative analysesvar} ± 1,8 \%$$
Disse konfidensintervaller er indtegnet for hvert punkt på Figur 1, og det ses, at holdbarheden er tvivlsom efter 3 døgn, da \(bias\%_{max}\) grænsen ligger indenfor konfidensintervallet på dette tidspunkt. En rimelig konklusion er derfor, at holdbarheden må indskrænkes til to døgn (med mindre tungtvejende praktiske omstændigheder taler imod det).
Vurdering af holdbarhed ved hjælp af de enkelte analysesvar og den tilladte totalfejl
I fremgangsmåden ovenfor vurderes den gennemsnitlige ændring i analysesvaret, når en stikprøve af patientprøver undersøges. Men selvom denne gennemsnitlige ændring er signifikant lavere end \(bias\%_{max}\), hvilket indikerer at prøvematerialet er holdbart, kan svaret fra en (eller flere) patientprøve(r) godt være ændret så meget, at det risikerer at have kliniske konsekvenser for patienten. Derfor bør en undersøgelse af holdbarhed også indeholde en vurdering af ændringen af analyseresultaterne for de enkelte patientprøver.
Først må det besluttes, hvor meget analyseresultatet for en patientprøve må ændres under opbevaring, uden at det risikerer at få kliniske konsekvenser for patienten. Et bud på denne tilladte ændring for den enkelte prøve er tilladt totalfejl (engelsk: allowable total error), der beregnes ud fra kravene til analysens korrekthed (\(bias\%_{max}\)) og præcision (\(CV\%_{max}\)), begge i procent:
$$\textit{Tilladt totalfejl}=1{,}65\cdot CV\%_{max}+bias\%_{max}$$
For at vurdere, om ændringerne i analyseresultaterne for de enkelte patientprøver på et tidspunkt overstiger den tilladte totalfejl, kan man lave et plot over de relative analysesvar for hver af de prøver, der indgår i holdbarhedsforsøget, og i samme plot indtegne de grænser, der defineres af den tilladte totalfejl.
Kun hvis der for alle prøver gælder, at den relative ændring i analysesvaret efter et givet tidsrum er mindre end den tilladte totalfejl, er prøvematerialet holdbart. Med andre ord: hvis den relative ændring for blot én prøve er større end den tilladte totalfejl, er prøvematerialet ikke holdbart i det pågældende tidsrum. Bemærk, at denne regel ikke hviler på en stringent statistisk vurdering, men udspringer af de kliniske krav til analysens nøjagtighed.
Eksempel – fortsat
I Figur 2 nedenfor ses de relative analysesvar for hver af de syv prøver, der indgår i holdbarhedsforsøget for P-ALAT, samt grænserne, der defineres af den tilladte totalfejl, beregnet til 26% med \(CV\%_{max}\) = 9% og \(bias\%_{max}\) = 11,4%. Som det ses, falder to prøver uden for grænserne efter fire døgns opbevaring, så for analysen P-ALAT bør prøverne efter denne vurdering maksimalt opbevares i tre døgn ved 21°C.
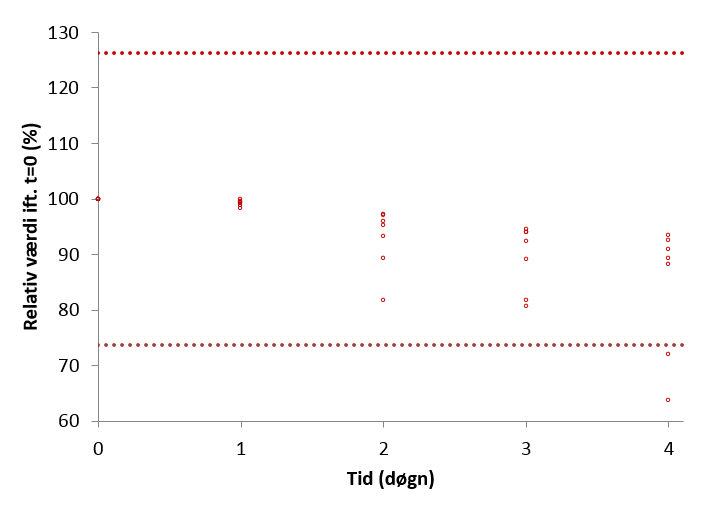
Figur 2. De relative analysesvar for for hver af de syv patientprøver efter opbevaring ved 21°C er vist med røde cirkler. Grænserne defineret af den tilladte totalfejl for analysen (±26%) er indtegnet som røde stiplede linier.
Praktiske overvejelser
Formålet med, at undersøge holdbarheden er, at vurdere, om opbevaring af prøvematerialet påvirker analyseresultatet. For at gennemføre undersøgelsen på den mest virkelighedstro måde, kan man opbevare prøvematerialet under de relevante omstændigheder (især temperatur og lysforhold) og analysere det efter de tidsintervaller, man har valgt. En ulempe ved dette forsøgsdesign kan dog være, at andet end opbevaring kan give anledning til forskelle i analyseresultaterne. Der kan fx blive skiftet reagens, kalibreret, udført service, eller på anden måde ændret ved analysen undervejs i undersøgelsen. For at udelukke disse forstyrrende variationskilder fra det endelige sæt af analyseresultater, bør man så vidt muligt benytte følgende fremgangsmåde:
- Prøvematerialerne fordeles i et antal portioner, så der er én portion til hvert tidspunkt i undersøgelsen. I eksemplet med P-ALAT ovenfor, skulle hver af de syv prøver altså fordeles i 5 portioner, svarende til tidspunkterne 0, 1, 2, 3 og 4 døgn.
- På de enkelte tidspunkter i undersøgelsen nedfryses en portion af hvert prøvemateriale, så hurtigt og så koldt som muligt.
- Efter at alle portioner er frosset ned (også den, der blev opbevaret længst), tøs de op samtidigt og analyseres i samme batch/serie.
På den måde minimeres den analytiske variations påvirkning af undersøgelsen. En vigtig forudsætning er dog, at komponenten, man undersøger, tåler nedfrysningen.
|